Istilah gas pertama kali digunakan pada permulaan abad ke-17 oleh seorang kimiawan bernama Flandria J.B. van Helmont. Gas adalah sampel materi yang sesuai dengan bentuk wadah tempat ia berada dan memperoleh kerapatan yang seragam di dalam wadah, bahkan di hadapan gravitasi dan terlepas dari jumlah zat dalam wadah.
Jika tidak terbatas pada wadah, materi gas, juga dikenal sebagai uap, akan menyebar ke seluruh ruang. Istilah gas juga digunakan sehubungan dengan wujud, atau kondisi, dari materi yang memiliki sifat ini. Contoh gas adalah oksigen pada suhu kamar (sekitar 20 ºC atau 68 ºF), hidrogen pada suhu kamar, dan air pada tekanan atmosfer standar dan suhu di atas 100 ºC atau 212 ºF.
Gas dalam Fisika
Arti atom atau makna molekul materi dalam bentuk gas bergerak bebas satu sama lain, dan, dalam banyak kasus, dikemas lebih longgar daripada molekul dari zat yang sama dalam keadaan padat atau cair. Sampel materi gas dapat dikompresi. Ketika sampel materi dalam bentuk gas dipanaskan, atom atau molekul memperoleh energi kinetik dan bergerak lebih cepat. Ketika sampel materi gas didinginkan, atom atau molekul kehilangan energi kinetik dan bergerak lebih lambat.
Jika sampel zat gas, terbatas pada wadah ukuran tetap, dipanaskan, tekanan meningkat. Jika sampel didinginkan, tekanan turun. Jika sampel zat gas ditempatkan dalam wadah bersegel dan kemudian volume wadah dikurangi, kompresi memanaskan gas. Jika volume wadah yang disegel meningkat, dekompresi mendinginkan gas.
Jika suhu menjadi cukup tinggi, gas-gas tertentu, seperti hidrogen, akan dengan cepat bergabung dengan gas-gas lain seperti oksigen atau klorin. Ini adalah pembakaran. Beberapa reaksi dalam arti kimia antara gas dan zat lain terjadi lebih lambat; contohnya adalah oksidasi besi secara bertahap untuk membentuk besi oksida (karat). Dalam hal ini, oksigen berbentuk gas pada suhu kamar, sedangkan besi dan oksida besi adalah padatan.
Ketika sampel materi dalam bentuk gas didinginkan hingga suhu yang cukup rendah, mungkin menjadi cairan atau padatan. Misalnya, jika nitrogen didinginkan pada suhu yang jauh di bawah nol Celcius, ia mencair.
Nitrogen cair digunakan oleh beberapa dokter untuk menghancurkan lesi kulit kecil seperti kutil. Gas lain, karbon dioksida, melewatkan fase cair ketika didinginkan pada tekanan atmosfer, dan menjadi padatan yang dikenal sebagai es kering.
Pengertian Gas
Gas adalah keadaan materi yang terdiri dari partikel-partikel yang tidak memiliki volume atau bentuk yang pasti. Ini adalah salah satu dari empat wujud mendasar materi, yang lainnya yaitu padatan, cairan, dan plasma. Dalam kondisi biasa, gas berupa materi yang bentuknya antara wujud cair dan plasma.
Gas murni dapat terdiri dari atom individu (misalnya Gas mulia seperti neon), molekul unsur yang terbuat dari satu jenis atom (mis. Oksigen), atau molekul senyawa yang dibuat dari berbagai atom (misisalnya Karbon dioksida).
Pengertian Gas Menurut Para Ahli
Adapun gas dalam definisi fisika menurut para ahli, antara lain:
Wikipedia
Gas ialah salah satu dari empat wujud dasar materi (yang lainnya yaitu padat, cairan, dan plasma). Gas murni bisa tersusun atas atom (misalnya gas mulia seperti neon), molekul elemen yang tersusun atas satu jenis atom (misalnya oksigen), atau molekul senyawa yang tersusun dari berbagai macam atom (misalnya karbon dioksida).
Your Dictionary
Gas adalah salah satu dari tiga kondisi materi, dua lainnya berbentuk cair dan padat. Banyak unsur ada sebagai gas pada suhu dan tekanan standar, sementara banyak unsur dan senyawa lain dapat menjadi gas dalam keadaan tertentu.
Sifat Gas
Sifat gas bisa dibedakanmenjadi dua, yaitu sifat kesetimbangan dan sifat-sifat pengangkutan. Berikut penjelasannya:
Sifat Kesetimbangan
Berdasarkan sifat ini, bisa dikatakan bahwa suatu sistem yang berada dalam kesetimbangan tidak akan mengalami perubahan kecuali karena adanya beberapa perlakuan eksternal yang dilakukan di atasnya (misalnya, menambahkan panas).
Dalam sifat ini, perilaku gas stabil dengan waktu, dan tidak terdapat perubahan tampak akan terjadi, meskipun molekul bergerak tanpa henti. Sebaliknya, sifat non-kesetimbangan menunjukkan bagaimana sistem merespon beberapa tindakan eksternal, seperti pengenaan suhu atau perbedaan tekanan.
Sifat kesetimbangan bisa dibedakan menjadi dua, yaitu:
- Persamaan Gas Ideal
Gas merupakan materi yang bersifat makroskopis (sifat dari besaran-besaran yang bisa diukur dengan alat ukur, misalnya suhu (T), tekanan (P), volume (V) dan mikroskopis (sifat dari besaran-besaran yang tidak dapat diukur secara langsung, misalnya kelajuan (v), energi kinetik (Ek), momentum (p), massa tiap partikel penyusun materi (m).
- Energi Dalam
Energi dalam (E) merupakan besarnya energi kinetik (energi yang ada dari tumbukan antar molekul) sebanyak partikel gas yang terdapat di dalam ruang. Masing-masing molekul gas bergerak dalam ruang tiga dimensi, dan gerak translasi ini berkontribusi (3/2) RT (per mol) energi dalam E.
Untuk gas monoatomik, misalnya helium, neon, argon, kripton, dan xenon, ini menyumbang energi tunggal. Gas yang mengandung dua atau lebih atom per molekul juga menyumbang masa tambahan sebab gerakan internal mereka, di mana Eint termasuk kontribusi dari rotasi molekul dan getaran internal.
Sifat Transportasi atau Pengangkutan
Sifat transportasi bisa dibedakan menjadi tiga, yaitu:
- Viskositas
Viskositas bisa didefinisikan sebagai gaya gesekan antara lapisan-lapisan yang bersisian pada fluida pada waktu lapisan-lapisan tersebut bergerak satu melewati lainnya. Viskositas terdapat pada zat cair maupun gas. Sebagai contoh yaitu air mempunayi viskositas yang lebih rendah dibandingkan madu.
- Konduktivitas Panas
Apabila konduksi panas perbedaan arti suhu dipertahankan di sebuah aliran fluida melalui fluida akan menghasilkan energi.
- Difusi
Difusi gas merupakan proses di mana partikel gas satu menyebar ke seluruh gas lain oleh gerak molekul. Sebagai contoh, ketika kita membuka botol parfum, baunya bisa sangat cepat tercium di seberang ruangan. Hal tersebut disebabkan karena sebagai partikel aroma arus keluar dari botol, molekul-molekul gas di udara berbenturan dengan partikel dan secara bertahap mendistribusikan mereka di seluruh udara.
Ciri Gas
Sebagian besar gas sulit untuk dapat diamati secara langsung. Oleh sebab itu, gas-gas tersebut dijelaskan melalui penggunaan empat sifat fisik atau karakteristik makroskopis, yaitu tekanan, volume, jumlah partikel (kelompok kimiawi berdasarkan mol) dan suhu.
Keempat karakteristik ini berulang kali diamati oleh para ilmuwan seperti Robert Boyle, Jacques Charles, John Dalton, Joseph Gay-Lussac dan Amedeo Avogadro untuk berbagai gas di berbagai lingkungan. Studi terperinci mereka akhirnya mengarah pada hubungan matematika antara sifat-sifat ini yang dinyatakan oleh hukum gas ideal, seperti yang telah dikatakan sebelumnya.
Karakteristik gas diantaranya yaitu:
- Partikel-partikel gas secara luas terpisah satu sama lain, dan akibatnya, memiliki ikatan antarmolekul yang lebih lemah daripada cairan atau padatan. Gaya antarmolekul ini dihasilkan dari interaksi elektrostatik antara partikel gas.
- Daerah bermuatan serupa dari partikel gas yang berbeda menolak, sementara daerah yang bermuatan berbeda dari partikel gas yang berbeda menarik satu sama lain; gas yang mengandung ion bermuatan permanen dikenal sebagai plasma.
- Senyawa gas memiliki ikatan kovalen polar yang mengandung ketidakseimbangan muatan permanen, sehingga mengalami gaya antarmolekul yang relatif kuat. Transien, muatan yang diinduksi secara acak ada pada ikatan molekul kovalen non-polar dan interaksi elektrostatik yang disebabkan oleh mereka disebut sebagai gaya Van der Waals.
- Interaksi gaya antarmolekul ini bervariasi dalam suatu zat yang menentukan banyak sifat fisik yang unik untuk setiap gas. Perbandingan titik didih untuk senyawa yang dibentuk oleh ikatan ionik dan kovalen membawa kita pada kesimpulan ini.
- Dibandingkan dengan keadaan materi lainnya, gas memiliki kerapatan dan viskositas yang rendah.
- Tekanan dan suhu mempengaruhi partikel dalam volume tertentu. Variasi dalam pemisahan dan kecepatan partikel ini disebut sebagai kompresibilitas. Pemisahan dan ukuran partikel tersebut berpengaruh terhadap sifat optik gas. Akhirnya, partikel gas menyebar terpisah atau berdifusi untuk mendistribusikan diri secara homogen ke seluruh wadah.
Rumus Gas
Dalam menentukan gas ideal, berlaku 3 hukum kinetika, gas, antara lain:
-
Hukum Boyle
Berbunyi: Apabila suhu gas yang terdapat di dalam bejana tertutup (tidak bocor) dijaga konstan, maka tekanan gas P (N/m2) akan berbanding terbalik dengan volumenya V (m3 ).
-
Hukum Charles
Berbunyi: Apabila tekanan gas yang terdapat di dalam bejana tertutup (tidak bocor) dijaga konstan, maka volume gas akan sebanding dengan suhu mutlaknya.
-
Hukum Avogadro
Berbungyi: Gas-gas yang mempunyai volume yang sama, pada suhu dan tekanan yang sama, memiliki jumlah molekul yang sama pula.
Berdasarkan ketiga hukum di atas, bisa dikatakan volume gas berbanding langsung terhadap jumlah gas dan suhu dan berbanding terbalik terhadap tekanan. Persamaa untuk menghitung gas ideal, yaitu:
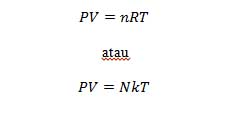
Keterangan:
- N : jumlah partikel gas
- n : jumlah mol gas
- R : tetapan gas umum, yaitu 8,31 x 103 M/mol K
- K : tetapan Boltzman, yaitu 1,38 x 10-23 J/K
Untuk menghitung jumlah mol gas (n) bisa dilakuakn melalui dua alternative rumus, yaitu:
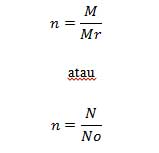
Keterangan:
- No : bilangan avogadro 6,02 x 1023
- Mr : massa molekul relatif gas
- M : masa partikel gas
Contoh Gas
Berikut ini beberapa contoh gas, antara lain:
-
Gas Beracun
Karbon monoksida adalah salah satu gas beracun yang membahayakan manusia dan hewan dengan mendorong oksigen ke atas. Dikenal dengan rumus CO, ia memiliki kerapatan yang lebih rendah daripada oksigen dan karenanya lebih mudah diakses tetapi tidak menyediakan oksigen yang cukup untuk bernafas.
-
Gas Elemental (Gas Unsur)
Sebelas unsur – hidrogen, nitrogen, oksigen, fluor, klor, helium, neon, argon, kripton, xenon, dan radon – ada sebagai gas di bawah tekanan dan suhu standar. Tergantung pada elemennya, ketika suhu atau tekanan dinaikkan atau diturunkan, maka gas-gas tersebut akan beralih ke keadaan lain.
-
Gas Murni
Gas murni tidak memiliki molekul gas lain yang bercampur dengannya. Salah satu contohnya adalah oksigen murni. Meskipun kita tidak menghirup oksigen murni karena atmosfer kita terdiri dari berbagai gas, pasien rumah sakit dengan kesulitan bernapas akan bernapas dengan oksigen murni untuk membantu paru-paru mereka mentransfer oksigen ke aliran darah secara lebih efisien.
-
Gas dalam Industri
Sejumlah gas campuran melayani keperluan industri di bidang manufaktur seperti pengelasan, produksi baja, pendinginan, propelan, dan banyak lagi. Asetilena, butana, propana, dan banyak gas lainnya bahkan digunakan dalam aplikasi rumah tangga sebagai sumber panas bersuhu tinggi.
Maka, itutadi artikel yang bisa kami tuliskan kepada segenap pembaca terkait dengan pengertian gas dalam fisika menurut para ahli, sifat, ciri, rumus, dan contohnya. Semoga memberikan wawasan sekaligus pengetahuan bagi semuanya. Trimakasih,




